Aliments et microbes : un engagement à vie
Une analyse des incidences du nouveau Guide alimentaire canadien sur les bactéries qui colonisent le corps humain
La composition de notre corps est tout aussi bactérienne qu’humaine; selon les estimations actuelles, nous hébergeons un nombre équivalent de cellules bactériennes et de cellules humaines.1 Nos cellules bactériennes résidentes – ainsi que d’autres microbes tels que les virus, les champignons et les levures – constituent notre microbiome. Nous comptons sur notre microbiome intestinal pour effectuer des fonctions essentielles à notre santé, telles que la décomposition d’aliments que nous ne pouvons digérer par nous-mêmes pour en obtenir de l’énergie, la production de vitamines, qui renforcent notre système immunitaire et la protection contre les infections par des bactéries néfastes (des pathogènes) comme celles qui causent un empoisonnement alimentaire.2
Nous avons fait d’énormes progrès au cours des dernières années au niveau de notre compréhension de la composition et de la fonction du microbiome humain, grâce à l’utilisation de technologies complexes de séquençage de l’ADN.3 Une part importante de l’analyse cherchant à définir ce qu’est un microbiome sain a porté sur les populations bactériennes, étant donné que celles-ci constituent la majeure partie de notre microbiome, étant de loin bien plus nombreuses que les autres microbes. Le microbiome intestinal a fait l’objet de recherches poussées puisque les altérations et le déséquilibre (la dysbiose) de la composition bactérienne à cet endroit sont associés à une variété de maladies, entre autres, la maladie inflammatoire de l’intestin (MII), le syndrome de l’intestin irritable (SII), l’asthme, les allergies, l’obésité et le diabète de types 1 et 2.4 Les associations entre les états pathologiques et la dysbiose bactérienne intestinale ont poussé davantage les chercheurs à vouloir comprendre les facteurs qui influent sur les populations bactériennes et, par conséquent, les répercussions de tels changements sur notre santé intestinale.
L’écosystème intestinal
Le tractus gastro-intestinal, notre plus grande surface liée au monde externe, est un tube qui traverse le corps, de la bouche à l’anus. Nos intestins constituent la plus grande partie du tractus gastro-intestinal et ont les incroyables tâches de digérer les aliments que l’on ingère, d’absorber les nutriments digérés et de former une barrière physique et immunitaire compétente, et ce, tout en abritant des billions de bactéries.5 Le microbiome intestinal se trouve dans la partie interne (la lumière) du tractus par lequel passent les aliments et les matières digérées. Les types de populations bactériennes qui sont aptes à habiter les différents espaces physiques le long des intestins découlent largement des facteurs environnementaux, y compris les produits libérés par les cellules intestinales et les aliments que nous mangeons.6
Le nombre de bactéries résidant dans le tractus gastro-intestinal augmente en passant de l’intestin grêle supérieur (duodénum→jéjunum→iléon) vers le gros intestin ou côlon.6 Le duodénum, où le contenu de l’estomac passe en premier, contient des bactéries qui se comptent par centaines. En revanche, les régions du côlon les plus éloignées de l’intestin grêle abritent des billions de bactéries. Cette densité accrue est attribuable à plusieurs facteurs environnementaux, dont une augmentation du pH (le milieu devient moins acide) dans la région du côlon. L’oxygène, dont la concentration est plus faible dans la région du côlon, a également une incidence sur la densité bactérienne, car il est effectivement toxique pour bon nombre de nos bactéries résidentes. De plus, le transit des matières digérées, beaucoup plus rapide dans la section de l’intestin grêle que dans le côlon, influence la capacité des bactéries à coloniser certaines sections avec succès.
Les cellules épithéliales qui agissent à titre d’interface entre la lumière et le tissu intestinal sous-jacent sont également source de facteurs qui agissent sur les bactéries.5 Par exemple, il existe dans l’intestin grêle un type de cellules épithéliales intestinales (les cellules de Paneth) qui est absent du côlon sain.7 Les cellules de Paneth sont de puissantes productrices de peptides antimicrobiens qu’elles libèrent dans la lumière, y limitant ainsi les populations bactériennes. Elles sont présentes en plus grand nombre dans le duodénum et en plus faible quantité dans l’iléon.
Par contre, les cellules caliciformes, un autre type de cellules épithéliales intestinales responsables de la production du mucus intestinal, sont présentes en plus grand nombre dans la région du côlon. 7 Par conséquent, l’épaisseur de la couche de mucus s’accroît en s’approchant du côlon – elle est à son maximum dans le côlon et à son minimum dans la partie supérieure de l’intestin grêle. La couche diffuse de mucus dans le duodénum et le jéjunum est nécessaire à l’absorption optimale des nutriments, tandis que la couche de mucus plus épaisse du côlon protège l’épithélium intestinal contre les selles compactes qui se déplacent dans la lumière, tout en fournissant un endroit aux bactéries résidentes pour s’installer ou y adhérer en plus grand nombre.8
Les bactéries intestinales dépendent de nous pour s’alimenter
Le deuxième facteur le plus important influant sur les populations bactériennes de l’intestin est la nourriture que nous consommons. Tout comme nos cellules, et par extension notre corps, ont besoin de l’énergie provenant des nutriments absorbés pour fonctionner, les bactéries ont besoin de nutriments pour survivre. Des nutriments précis sont absorbés à différents endroits de l’intestin humain. Ce processus influence à son tour les nutriments accessibles aux bactéries colonisant le lumen. Par exemple, la majorité des produits provenant de la décomposition des glucides digestibles (les sucres simples) sont absorbés par l’intestin grêle.6 Par conséquent, les bactéries résidant dans le côlon doivent être capables d’utiliser les glucides complexes non digestibles par le corps pour en tirer de l’énergie, puisqu’une fois les aliments rendus au côlon, la plupart des sucres simples ont été absorbés. Consultez le tableau 1 ci-dessous pour un survol des endroits de l’intestin où les différents nutriments sont absorbés.
| Nutriments | Site d’absorption |
| calcium, fer, produits de la décomposition des glucides (glucose), vitamines liposolubles (A et D) | duodénum |
| graisses, produits de la décomposition des glucides (sucrose, glucose, lactose), magnésium, vitamines liposolubles (A et D), protéines (acides aminés) | jéjunum |
| protéines (acides aminés), magnésium, vitamine B12, fer | iléon |
| eau, potassium, chlorure de sodium, sous-produits de la digestion bactérienne | côlon |
| Tableau 1.9 | |
La capacité des bactéries à utiliser les nutriments présents dépend des outils dont elles disposent pour les décomposer en forme consommable. C’est Darwin qui a le mieux illustré ce concept en décrivant les pinsons qu’il découvrit sur les îles Galápagos. Darwin a observé une douzaine d’espèces d’oiseaux étroitement liés, chez lesquels il existait des différences remarquables au niveau de la taille et de la forme du bec, celui-ci étant hautement adapté à leur source particulière de nourriture se trouvant sur les différentes îles.10 Par exemple, ceux qui se régalaient des graines et de la pulpe de fruits de cactus utilisaient leur long bec pointu pour consommer leur nourriture, alors que ceux dont le bec était plus court mangeaient des graines et des larves d’insectes près de la base des cactus. Plutôt que des becs, les bactéries emploient des enzymes ou protéines pour décomposer différents nutriments en une forme utilisable d’énergie.11
Par l’entremise du processus de décomposition des nutriments, les bactéries produisent également de nombreux sous-produits.2 Ceux-ci comprennent des gaz, comme l’hydrogène et le méthane, des vitamines comme la vitamine K et celles du groupe B (nous comptons sur les bactéries pour en être la source), et des métabolites tels que les acides gras à chaîne courte (AGCC). Les AGCC sont une source importante d’énergie pour les cellules épithéliales intestinales de notre côlon et ils peuvent aussi servir à calmer le système immunitaire.12
Acides gras à chaîne courte (AGCC)
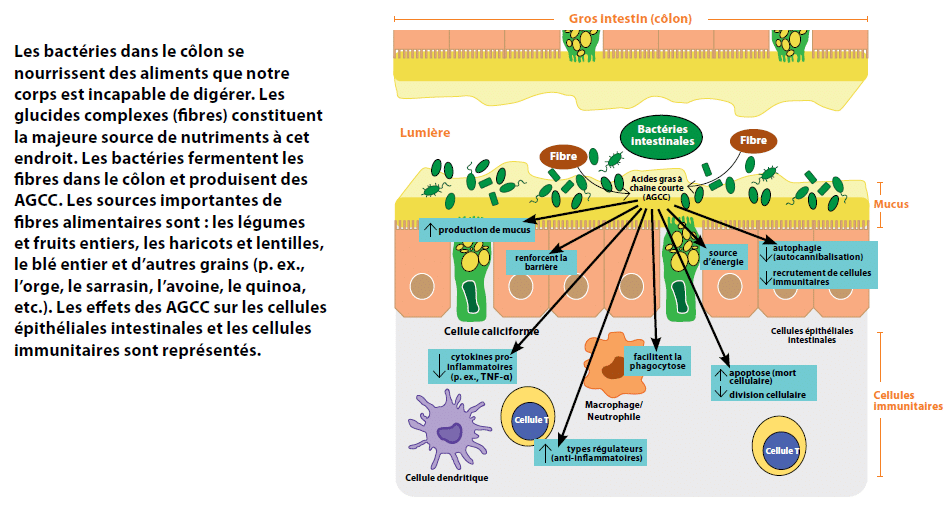
Les AGCC sont les produits finaux du métabolisme des sucres en l’absence d’oxygène (la fermentation). Les bactéries du côlon peuvent décomposer les glucides complexes en une forme fermentescible à l’aide d’enzymes telles que les polysaccharides lyases, produisant ainsi de grandes quantités d’AGCC.13 Les bactéries se nourrissant de l’abondant mucus intestinal du côlon au moyen d’enzymes spécialisées comme les glycosidases, produisent ainsi elles aussi des AGFC. Les AGCC les plus abondants sont le butyrate, le propionate et l’acétate, qui constituent une source importante de nutriments pour les cellules épithéliales intestinales. Des études menées chez des rats nés et hébergés dans un environnement stérile et n’ayant aucun microorganisme à la surface ou à l’intérieur de leur corps (ils sont exempts de germes) ont révélé que ces rats devaient augmenter leur apport alimentaire de 30 % afin d’extraire une même quantité d’énergie des aliments ingérés, cela étant attribuable à l’absence de bactéries.14
Au cours des quelques dernières années, les AGCC ont également été reconnus pour leur capacité à influencer les réponses immunitaires et à renforcer la barrière intestinale.15 Les AGCC peuvent entrer en jeu au niveau des cellules épithéliales intestinales pour améliorer la fonction de la barrière intestinale en renforçant les jonctions entre les cellules,16 améliorer la production de mucus,17 réduire l’autocannibalisation cellulaire causée par la carence en nutriments (l’autophagie), préservant ainsi la barrière intestinale,18 et réduire la libération de protéines de signalisation (cytokines et chimiokines) qui recrutent des cellules immunitaires pro-inflammatoires.2 Les AGCC peuvent également agir sur les cellules immunitaires sous-jacentes des cellules épithéliales intestinales. Par exemple, l’exposition des neutrophiles, type de cellule immunitaire, à l’acétate ou au propionate facilite leur capacité à engloutir et à détruire les bactéries (la phagocytose). Les AGCC suppriment la capacité d’autres types de cellules immunitaires à produire des cytokines pro-inflammatoires telles que le TNF-a en l’absence de stimulus inflammatoires.2 De plus, les AGCC peuvent entraîner les cellules T, type de globule blanc, à se transformer en lymphocytes T régulateurs et lymphocytes T anti-inflammatoires, tout en incitant les cellules T de nature plus réactive et inflammatoire à ralentir leur division cellulaire et en provoquant chez elles un taux accru de mort cellulaire (l’apoptose).2
Tout cela démontre que les bactéries sont décidément très utiles à l’appareil digestif.
Bactéries du microbiome intestinal humain
À un niveau élevé de la nomenclature, l’on regroupe les bactéries en une trentaine (bien que l’on postule qu’il en existe une centaine) d’embranchements (ou phylums) officiellement décrits.1 En comparaison, il existe environ trente-six embranchements dans le règne animal.20 La majorité des bactéries qui forment le microbiome intestinal appartiennent à quatre des embranchements bactériens. Dans un intestin adulte en bonne santé, la plupart des bactéries présentes (environ 90 %) appartiennent aux embranchements des Firmicutes et des Bacteroidetes, avec un petit nombre étant classé sous les Actinobacteria et les Proteobacteria.21 En présence d’une maladie telle que la MII, ces proportions peuvent changer, c’est-à-dire qu’il peut y avoir une diminution des Firmicutes et une augmentation des Proteobacteria.
Si l’on se penche sur des organismes plus étroitement liés au sein de chaque embranchement, c’est-à-dire au niveau du genre, l’on observe des groupes de bactéries reconnus pour leurs effets probiotiques, ou bénéfiques. L’on compte parmi eux des bactéries des genres Lactobacilli, Bifidobacteria et Roseburia, ainsi que les espèces Faecalibacterium prausnitzii et Akkermansia mucinophila.22 Il n’est pas surprenant de constater que bon nombre des bactéries probiotiques énumérées ci-dessus sont de copieuses productrices d’AGCC, l’une des façons par lesquelles elles exercent leurs effets bénéfiques. Les personnes atteintes de la MII possèdent une quantité moindre de ces bactéries bénéfiques et, dans l’ensemble, une plus faible diversité bactérienne. De plus, leurs intestins abritent une plus grande quantité d’organismes comme Escherichia coli, membre de l’embranchement des Proteobacteria.21
Comment les modifications proposées au Guide alimentaire canadien influeront-elles sur nos bactéries?
Les fibres constituent un exemple d’un glucide complexe consommé par les humains. Un apport accru en fibres a été associé à une baisse du cholestérol, aussi bien qu’à un risque réduit de développer un cancer colorectal.23 Nos bactéries intestinales possèdent des enzymes pour digérer les fibres; alors, en augmentant notre consommation de fibres, nous leur fournissons davantage de nourriture à fermenter, entraînant une plus grande production du sous-produit d’AGCC. Chez les humains, un régime riche en fibres a été lié à une augmentation des bactéries bénéfiques comme les bifidobactéries et les lactobacilles. La consommation de suppléments concentrés renfermant des prébiotiques (ingrédients non digestibles par le corps et favorisant la croissance de bactéries bénéfiques) comme l’inuline peut aussi faire croître les populations de bifidobactéries et de l’organisme F. prausnitzii. Les prébiotiques tels que l’inuline se retrouvent dans les aliments comme les bananes vertes, les légumineuses, les poireaux, les asperges et les algues. Un manque de fibres dans le régime, qui a été étudié chez des modèles animaux, peut faire croître les bactéries intestinales qui décomposent le mucus intestinal et s’en nourrissent, donnant lieu à une plus mince couche de mucus et perturbant possiblement la barrière.24
En ce qui a trait aux protéines, le nouveau guide alimentaire encourage la consommation d’une plus grande quantité de protéines végétales plutôt que de protéines animales. Ce changement s’explique du fait qu’il existe une association entre la consommation de viandes rouges et transformées, et un risque accru de cancer colorectal, et que les protéines de soya sont liées à l’abaissement des taux de cholestérol.23 Une étude à court terme menée sur des sujets humains, publiée dans la revue Nature, a examiné les effets de régimes à base de produits exclusivement d’origine animale et exclusivement végétariens sur les bactéries intestinales – des résultats remarquables ont été observés après seulement cinq jours.25 Les régimes alimentaires à base de produits d’origine animale, composés de viandes, d’œufs et de fromages, ont entraîné une augmentation du nombre de bactéries associées à l’inflammation, ainsi qu’une diminution du nombre d’organismes appartenant aux Firmicutes, comme les bactéries du genre Roseburia, qui peuvent digérer les fibres végétales. En revanche, l’on a observé chez les personnes suivant un régime végétarien, riche en légumineuses, en céréales, en fruits et en légumes, une présence accrue des organismes du genre Roseburia et F. prausnitzii, ainsi qu’une concentration deux fois plus élevée de deux types d’AGCC, le butyrate et l’acétate, dans leurs selles. Il est intéressant de noter que la flore intestinale des personnes consommant un régime alimentaire à base de produits d’origine animale a été rétablie à sa composition bactérienne originale deux jours après l’arrêt du régime.
Les graisses existent sous de nombreuses formes, et il y a des preuves qui suggèrent qu’une consommation élevée de graisses saturées (celles qui sont généralement solides à la température ambiante) peut entraîner un risque accru de développer une maladie cardiovasculaire.23 Les effets des régimes riches en graisses sur les bactéries intestinales ont surtout été examinés dans des modèles animaux. Chez les souris de laboratoire nourries selon un régime riche en graisses contenant un plus grand pourcentage de graisses saturées, l’on observe des changements au niveau des espèces bactériennes intestinales, notamment une diminution des Bacteroidetes et une augmentation des Firmicutes, ainsi qu’une diminution de la diversité globale des espèces bactériennes.26 Dans un modèle chez le rat, une alimentation riche en graisses a également entraîné une réduction des niveaux d’AGCC dans les selles.27
Il est bien connu que le sucre est associé à un risque accru du développement de diabète et d’obésité.23 La consommation de boissons sucrées chez les enfants est également liée à une augmentation de dépôts de graisse (adiposité).28 Par conséquent, le Guide alimentaire recommande de consommer le sucre en faible quantité. La consommation de sucre et de certains édulcorants artificiels chez les souris de laboratoire ainsi que chez les sujets humains peut entraîner chez ceux-ci une dysbiose des bactéries intestinales.29 Les rats nourris selon un régime à haute teneur en sucre ont connu une augmentation de la population d’E. coli dans leurs intestins.27 Fait intéressant, les espèces bactériennes observées chez les souris nourries au moyen d’un régime riche en graisses et en sucre causent une obésité chez des souris ayant été préalablement exemptes de microbes et non obèses.30>
Données probantes du monde réel
Les meilleures données concrètes tirées du monde réel et visant les effets de l’alimentation sur la composition du microbiome intestinal humain proviennent de la comparaison de populations ayant des régimes alimentaires sensiblement différents. Dans le cadre d’une étude, des chercheurs ont comparé les microbiomes intestinaux d’enfants d’un village rural du Burkina Faso à ceux d’enfants vivant à Florence, en Italie.31 Le régime alimentaire des enfants africains est faible en gras et en protéines animales et se compose principalement de légumineuses, de céréales et de légumes, alors que les enfants italiens consomment un régime plus riche en protéines animales, en sucre, en amidon et en gras, et beaucoup plus faible en fibres. Les principaux embranchements de bactéries intestinales chez ces deux cohortes d’enfants présentaient des rapports manifestement différents. De plus, le microbiome intestinal des enfants italiens ressemblait de près à celui des souris de laboratoire nourries au moyen d’un régime riche en graisses et en sucre. Chose étonnante, les enfants de la cohorte africaine abritaient des espèces bactériennes précises, entièrement absentes chez les enfants italiens, pouvant dégrader au moyen d’enzymes un composant des parois cellulaires végétales (la cellulose), permettant à leur hôte d’obtenir un maximum d’énergie des fibres végétales. Les intestins de ces enfants étaient aussi colonisés d’une bien plus grande diversité bactérienne. En outre, les niveaux des principaux AGCC comme le butyrate et le propionate étaient quatre fois plus élevés dans les selles des enfants africains que dans celles des enfants italiens. Cette étude démontre clairement l’influence du régime alimentaire sur le microbiome intestinal dans les populations humaines.
Conclusion
Dans l’ensemble, les changements apportés au nouveau Guide alimentaire canadien devraient avoir des effets bénéfiques sur nos populations bactériennes intestinales et, par conséquent, sur notre santé gastro-intestinale. Les bactéries plus susceptibles de profiter à long terme d’une consommation accrue de légumes, de fruits, d’aliments à grains entiers et de protéines végétales sont celles qui assurent l’intégrité de la barrière intestinale et encouragent la présence de cellules immunitaires anti-inflammatoires. Nous sommes ce que nous mangeons, et il semble que nos bactéries le soient aussi.














